
前言:
我们知道,细胞体外培养时需要在培养基中加入血清,以维持细胞的生长和存活。而血清,尤其是牛血清,因成分复杂、批间差大和存在病原体污染的可能性等原因广为科研和生物制药用户所诟病,因此人们对不添加血清的培养基,即无血清培养基的需求日益增加。无血清培养基中不含血清,为能够实现与含血清培养基相似的维持和促进细胞生长的功能,其中必须添加白蛋白(Albumin)、胰岛素(Insulin) 和转铁蛋白(Transferrin)等营养成分来替代血清。
白蛋白可与维生素(如VB6),脂肪酸(如油酸、亚油酸和花生四烯酸等),以及离子(如铜离子)等结合,提高这些分子在细胞培养液中的溶解度,并使它们保持在稳定状态,以及防止被氧化。
胰岛素可维持无血清细胞培养液中细胞的生长,调节细胞对葡萄糖、氨基酸和脂肪酸的摄取、利用和贮存,同时抑制糖原、蛋白质和脂肪的分解。胰岛素也具有对抗细胞凋亡的作用。
转铁蛋白则是通用的铁转运剂,其可通过帮助细胞调节对铁的摄取量而维持细胞的稳态,进而有利于细胞的生长和增殖。
本文将对无血清培养基添加物:胰岛素,胰岛素的类似物--长型胰岛素样生长因子(Long R3 IGF-I),和转铁蛋白作以简单介绍和初步探讨,以期为配制无血清培养基提供一些思路。
第一部分:胰岛素(Insulin)
1. 什么是胰岛素?
胰岛素的英文名为Insulin,是由加拿大人弗雷德里克•格兰特•班廷爵士(Sir Frederick Grant Banting)和查尔思•贝斯特(Charles H Best)于1921 年发现的,因其特异性由胰岛β细胞分泌而得名。胰岛素的发现为人类治疗糖尿病带来了福音。
胰岛素是一种多肽类激素,由A、B 两条肽链组成。人胰岛素的A 链和B 链分别含21个氨基酸和30 个氨基酸,其中A7(Cys)-B7(Cys)、A20(Cys)-B19(Cys)四个半胱氨酸中的巯基形成两个二硫键,将A、B 两条链连接起来。
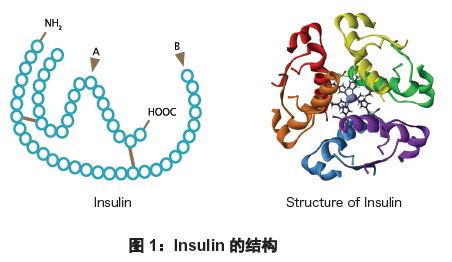
胰岛素基因位于染色体11P15.5,含3 个外显子和2 个内含子。生物合成时,编码胰岛素的基因在胰岛β 细胞的细胞核中先转录成446 bp 的mRNA,然后翻译成由105 个氨基酸相连的长肽,即前胰岛素原。前胰岛素原经过蛋白水解作用将前肽切除,生成由86 个氨基酸组成的长肽链--胰岛素原。胰岛素原在高尔基体中经蛋白水解酶的作用,切去第31、32 和60 位三个精氨酸连接的链,形成由A 链和B 链组成的胰岛素,然后分泌到胰岛β 细胞外,进入血液循环。
胰岛素的体外获得主要有提取和基因重组两种方式,人工合成胰岛素则是由中国科学家在1965 年首先实现的,当时合成出具有全部生物活力的结晶牛胰岛素,这也是第一个在实验室中用人工方法合成的蛋白质。
2. 胰岛素在无血清培养基中的作用
无血清或低血清培养基中,胰岛素为必加组分,这是由胰岛素对细胞的重要作用决定的。我们都知道,胰岛素在体内最主要的功能是调节机体血糖水平。其实胰岛素的作用非常广泛,包括调节蛋白质和脂肪的代谢,以及促进细胞生长等。
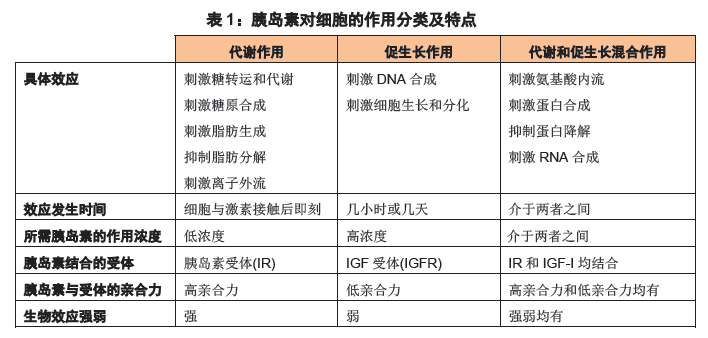
胰岛素功能的发挥源于其对细胞的作用,进而引起组织乃至机体的整体反应。我们可将胰岛素在细胞水平的广泛作用分为三大类:代谢作用、促生长作用、以及代谢和促生长混合作用(表1)。
与其他肽类激素、细胞因子以及神经递质相似,胰岛素首先与细胞膜上的特异性受体结合,然后启动各种生物学效应[图2] 。比较特殊的是,胰岛素的受体并不仅仅存在于特异性的靶组织,即胰岛β细胞上,而是普遍存在于几乎所有哺乳动物细胞上,只是不同细胞上胰岛素受体的数量会有差异。因此,胰岛素可被用于几乎所有细胞的无血清培养基的配制中。
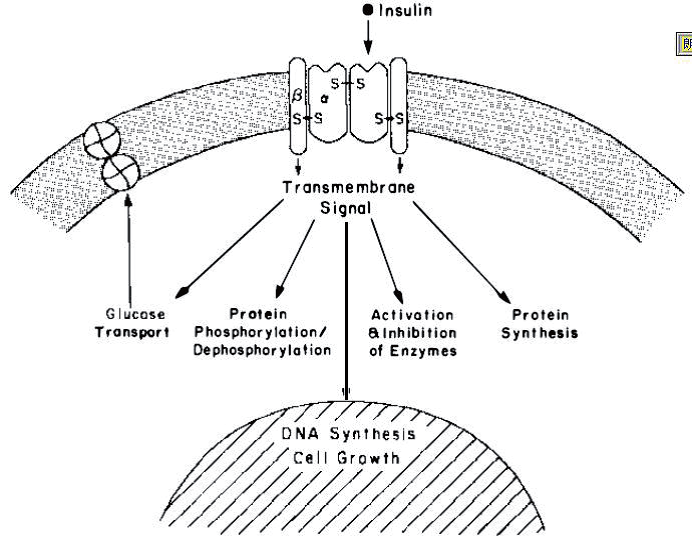 |
| 图2:胰岛素与细胞膜上受体的相互作用及生物学效应 |
| (摘自文献Kahn CR. Annu Rev Med. 1985;36:429-51[1]) |
需要注意的是,胰岛素对细胞的代谢调节作用主要是通过其与细胞膜上的胰岛素受体(Insulin receptor, IR)相互作用而介导,而胰岛素对细胞的促生长作用则是通过其与细胞膜上胰岛素样生长因子(Insulin-like growth factors, IGFs)的受体,即IGF Receptor (IGFR)相互作用而介导的。
3. 无血清培养基中应该添加提取的胰岛素,还是重组的胰岛素?
人胰岛素的来源有限,无法满足临床和科研的需求,因此人们通常从牛或猪的胰脏中提取获得胰岛素。
胰岛素种属间高度保守,猪和牛的胰岛素与人的胰岛素氨基酸序列上分别仅有1个和3个氨基酸的差异,所以猪和牛的胰岛素完全可以替代人的胰岛素来进行科学实验和临床治疗。
然而,毕竟猪和牛的胰岛素属异种蛋白,进入人体后容易产生抗体,影响治疗效果,并引起副反应。所以,目前临床上广泛应用的是重组人胰岛素,即使用基因工程手段,将人的胰岛素基因转移到细菌或者酵母细胞中,然后利用发酵工艺,进行大规模的生产,从而得到大量、高纯度的人胰岛素。
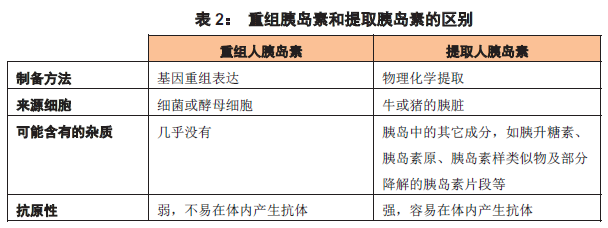
从表2 可以看出,提取的胰岛素可能含有其它激素等杂质,并可能因其异源性而导致在人体内产生抗体。所以,在配制无血清培养基时最好使用重组的人胰岛素,这样:
1) 如果此无血清培养基用于科学研究,不会因含有胰岛素以外的激素而引起与预期结果不符的反应;
2) 如果此无血清培养基用于细胞治疗,因无异源性,细胞体外培养后回输到人体时不会产生抗体,也就不会影响治疗的效果。
4. 无血清培养基中应该添加试剂级别的重组人胰岛素,还是药物级别的重组人胰岛素?
因为胰岛素具有治疗糖尿病的重要功效,所以多年前就已被制备成药品,以供糖尿病患者的使用。
药品确实具有制备严格(多数遵循GMP 标准生产),副作用和安全风险小等优点,因此许多无血清培养基生产厂家倾向于使用药物级别的胰岛素。然而,仍有不少厂家在使用试剂级别的重组人胰岛素来生产无血清培养基。
那么,无血清培养基究竟是该用试剂级别的重组人胰岛素,还是药物级别的重组人胰岛素呢?
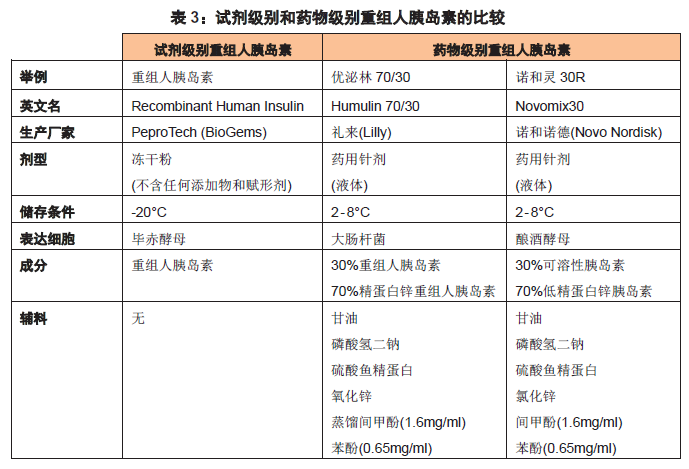
药品与试剂不同,药品有不同的剂型,如片剂、针剂、胶囊剂和栓剂等十多种。即使对于同一种剂型,其中还可分为若干亚型,如针剂包括注射水针剂、注射油针剂、中草药注射剂,以及注射用灭菌粉末等。而且药品通常保存于室温或2 - 8°C。这就要求药品在制备过程中除了包含药物本身(通常称为主药)外,还必须加入一些有助于制剂成型(如赋形剂)、稳定(如抑菌剂)、增溶和助溶等具有不同作用的辅料,也就是说药品中含有很多非药品成分。将药品添加入无血清培养基中进行细胞培养时,不可避免地会引入诸多不确定的因素,一方面可能会对细胞的生长或分化产生影响,另一方面可能会带来非预期的实验结果。而药物辅料对培养细胞的作用又很难通过设立辅料对照来确定,因为辅料的成分过于复杂,且通常药厂并不公开辅料的具体组分。
下面我们以药物级别的重组人胰岛素为例来看一下辅料对体外细胞培养的可能影响。
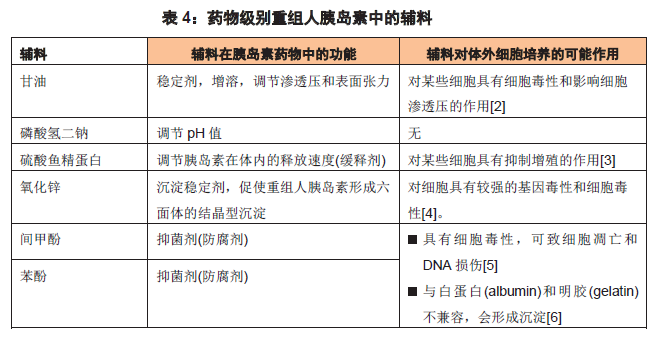
从上表可以看出,胰岛素药物中的辅料均具有一定的负面生物学功能,这些功能在药物用于人体内治疗时不会显现,因为人体具有肝脏等解毒器官,低浓度的有害物质短期内不会对人体的组织产生影响。但当药物用于体外细胞培养时,因为药物中的辅料会直接、完全地作用于细胞,这些辅料的副作用更容易显现出来。虽然当药物加入细胞培养体系时,辅料的浓度可能已经降得很低,但不排除这些辅料或多或少仍会对细胞的生长或分化产生某些影响。
另外,无血清培养基体系中所必须添加的组分-白蛋白(albumin) 与胰岛素药物中的辅料-苯酚和间甲酚会形成沉淀,从而在一定程度上影响白蛋白的功能。其实,已经证实苯酚的衍生物- 酚红(phenol red) 有干扰某些细胞的克隆性生长的作用,所以用于培养干细胞或生长密度比较低的细胞的无血清培养基中通常不添加酚红,尽管培养基中因此会缺少酸碱指示剂。
综上所述,配制用于体外细胞培养的无血清培养基最好使用不含任何辅料的试剂级别胰岛素,以避免辅料可能给细胞带来的危害以及实验结果不确定性的增加。
5. 胰岛素在无血清培养基中的使用浓度
所培养的细胞不同,无血清培养基中所需的胰岛素量也有所区别,一般在1-10mg/L之间。
药物级别的胰岛素一般以IU(International Units),即国际单位来表示其中胰岛素的含量。如果原来在无血清培养基中添加的是药物级别的胰岛素,现在想转换成试剂级别的胰岛素,么应该在每L 培养基中加入多少mg 的胰岛素呢?
药物胰岛素的一个IU 相当于6nmol,即0.035mg 的胰岛素。以礼来公司的优泌林70/30(Humulin 70/30) 400U/10mL 胰岛素为例,如果在配制某种无血清培养基时,每L 加入10U,那么转换为使用试剂级别的胰岛素时,则每L 需加入:10 x 0.035mg = 0.35mg 的试剂级别胰岛素。
第二部分:Long R3 IGF-I 优于胰岛素和IGF-I
1. IGF-I与胰岛素
IGF-I 是IGFs 的一种。IGFs 的英文全称是Insulin-like growth factors,即胰岛素样生长因子,因其可模拟胰岛素对细胞的全部生物学效应而得名。
IGFs 与胰岛素在功能上基本相同,但胰岛素主要作用于细胞的代谢,而IGFs 主要作用于细胞的生长。
IGFs 包括IGF-I 和IGF-II 两种低分子量多肽,分别由70 和67个氨基酸组成,两者氨基酸的一致性为62%,与胰岛素有约50%的氨基酸是一致的。
在无血清培养基的配制中,常用IGF-I 来替代胰岛素,原因是IGF-I 在很低的浓度即可实现或超过远远高于生理浓度的胰岛素的促细胞生长作用。
2. 什么是Long R3 IGF-I?
Long R3 IGF-I 是人IGF-I(胰岛素样生长因子-I)的重组类似物。
从结构上来讲,Long R3 IGF-I 可称为长型IGF-I,因为其是将IGF-I 全长氨基酸序列的第3 位谷氨酸(G)变为精氨酸(R),并在N 端添加一段长为13 个氨基酸的肽链。由此可知,Long代表N 端加长,而R3 代表第3位氨基酸变为精氨酸(R)。

从效用上来讲,Long R3 IGF-I 可称为长效IGF-I,因为与胰岛素相比,Long R3 IGF-I添加到无血清培养基中后不容易被降解,所以作用更持久。
3. Long R3 IGF-I与胰岛素、IGF-I 的比较
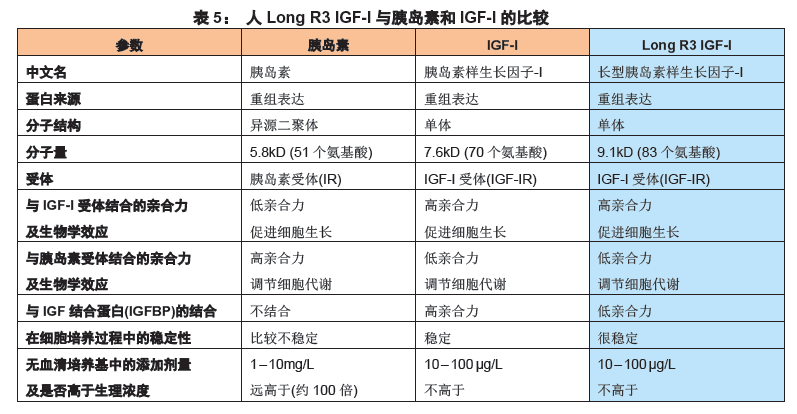
4. Long R3 IGF-I优于胰岛素
1) 促细胞增殖能力更强
从表5 和图4 可以看出,细胞表面的胰岛素受体(Insulin Receptor,IR)主要介导对细胞的代谢调节作用,而IGF-I 受体(IGF-I Receptor,IGF-IR)主要介导促细胞生长作用。
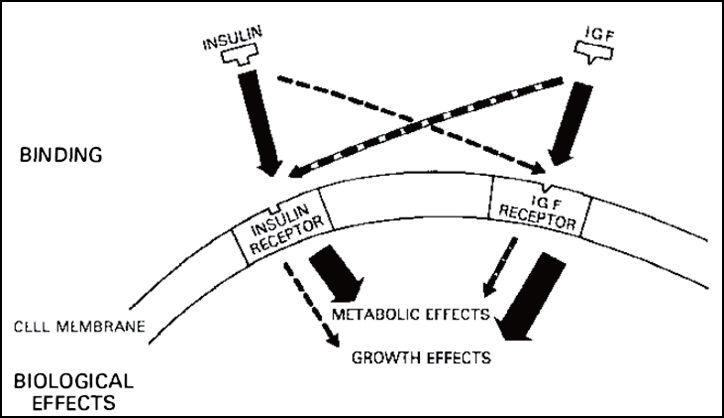 |
| 图4:胰岛素和IGF 与受体的结合及产生的生物学效应 |
| (摘自文献Kahn CR. Annu Rev Med. 1985;36:429-51[1]) |
与胰岛素的受体相似,IGF-I 的受体也存在于大多数细胞的细胞膜上,因此多数情况下,同一细胞上会既存在胰岛素的受体,又存在IGF-I 的受体。更需注意的是,胰岛素和IGF-I 除可与各自的相应特异性受体, IR和IGF-IR结合并介导相应的生物学效应(分别为代谢调节和促生长作用),也可与对方的受体结合,即胰岛素可以与IGF-IR结合,介导促细胞生长和增殖作用,而IGF-I 也可与IR 结合,介导对细胞代谢的调节作用,只是与相应特异性受体结合的亲合力很高,而与对方受体结合的亲合力很弱,也就导致胰岛素和IGF-I 通过特异性受体产生的生物学效应较强,而通过对方受体产生的生物学效应较弱。总结如下:
a. 胰岛素的主要作用是调节细胞的代谢,虽然也具有促进细胞生长作用,但较弱,这也正是在无血清培养基中需要添加远高于生理浓度的胰岛素(高于生理浓度100 倍之多,浓度一般为1 - 10mg/L)才能维持细胞生长的原因。
b. IGF-I 的主要作用是促进细胞生长,也具有调节细胞代谢的作用,但较弱。因此,很低浓度的IGF-I(10 -100μg/L) 即可维持无血清培养液中细胞的生长。
此外,有些细胞,如CHO(中国仓鼠卵巢细胞)等细胞上,IR 的数量很少,而IGF-IR的数量较多(表6),因胰岛素是通过与IGF-IR 结合来发挥促细胞生长作用的,所以如果无血清培养基中添加的是胰岛素,即使所用的胰岛素浓度再高,因其与IGF-IR受体的亲合力较弱,仍无法达到与IGF-I 等同的促细胞生长效应。此时的最佳策略是直接在无血清培养基中添加IGF-I ,这样细胞的生长会得到非常好的维持,而且IGF-I 的使用浓度也很低。
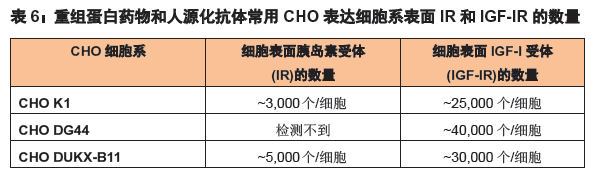
Long R3 IGF-I 是在全长IGF-I 的基础上重组表达而得的,因此与IGF-I 受体的特异性结合能力不比IGF-I 差,产生的生物学效应也相同。对于某些细胞,在无血清培养基中添加Long R3 IGF-I 的剂量即使仅为胰岛素的1/200,也可实现远好于胰岛素的促进细胞生长和增殖作用。
2) 细胞密度更高,细胞活力更好
工业级别细胞培养一般是在生物反应器中进行的,其中,应激(stress)诱导的凋亡是细胞丧失活力的主要原因。Long R3 IGF-I 通过活化IGF-IR 受体可引起多个信号转导通路的激活,这对细胞的存活和增殖至关重要。与胰岛素相比,Long R3 IGF-I 对IGF-IR 的活化能力更强,其激活某些关键抗凋亡和增殖信号分子(如Akt 和MAPK 等) 的能力也更强。这些信号分子的激活可防止因培养条件和环境的变化而引起的细胞活力丧失。
因此,与胰岛素相比,添加Long R3 IGF-I 的无血清细胞培养基所培养出的细胞密度更高,活细胞数更多。
3) 提高重组蛋白或抗体的产量
从第1)和第2)点可以看出,用Long R3 IGF-I 培养的细胞增殖能力强,活细胞数目多,所以用添加Long R3 IGF-I 的无血清细胞培养基培养表达重组蛋白或抗体的细胞时,通常会比用添加胰岛素的无血清细胞培养基培养获得更高产量的重组蛋白或抗体。
也就是说,如果目的是生产重组蛋白或抗体,最好用添加Long R3 IGF-I 的无血清细胞培养基来优化一下生产流程,有可能会使生产效率得以明显提高。
4) 培养液中半衰期更长,生物活性更长效
细胞在培养过程中会内化培养液中所添加的生长因子,同时也会分泌一些酶到培养基中,引起生长因子的降解。与胰岛素相比,Long R3 IGF-I 更加稳定,被细胞内化和酶降解的速度较慢,因此其在培养体系中的半衰期更长,生物学活性发挥更持久,细胞的培养效果也更好。
在正常的细胞培养条件下,Long R3 IGF-I 比胰岛素的有效作用时间最长可延长2倍之多,因此Long R3 IGF-I 又可称为长效IGF-I。
5. Long R3 IGF-I优于IGF-I
Long R3 IGF-I 是以IGF-I 为基础改造而来,即IGF-I 的氨基酸序列中第3 位谷氨酸(G)被精氨酸(R)所取代,而且在氨基末端加了一个13 个氨基酸的延长肽。改造后,Long R3IGF-I 仍具有高亲合力结合IGF-IR 的能力,因此保持着与IGF-I 相似的促细胞增殖活性。同时,改造给Long R3 IGF-I 带来一个非常显著的优点,即与IGF 结合蛋白(IGF Binding Proteins, IGFBPs)的亲合力明显下降。
所有哺乳动物细胞均会分泌IGFBPs,后者可结合并抑制IGF-I 的活性,而改造后的Long R3 IGF-I 与IGFBPs 的亲合力比其原型分子IGF-I 下降1000 多倍,因此其活性可极大程度地避免被IGFBPs 所抑制,从而使得Long R3 IGF-I 在培养体系中的生物可利用度和活性较IGF-I 大为提高。
综上所述,Long R3 IGF-I 是IGF-I 的升级版本,具有诸多重要的优点,原来添加胰岛素或IGF-I 的无血清培养基可尝试使用Long R3 IGF-I,或许会获得更好、更稳定的细胞培养效果。
第三部分:转铁蛋白(Transferrin)
1. 什么是转铁蛋白?
转铁蛋白的英文名为Transferrin,简称TF,是血浆中主要的含铁蛋白质,负责运载由消化管吸收的铁和由红细胞降解释放的铁。以三价铁复合物的形式进入骨髓中,供成熟红细胞的生成。
转铁蛋白是机体不可或缺的蛋白,其不仅参与铁的运输与代谢,从而调节铁离子平衡和能量平衡,还参与呼吸、细胞增殖和免疫系统的调节,更具有抗菌杀菌的保护功能。
转铁蛋白主要存在于血浆中,在网状细胞、胎盘、粘膜、卵巢、睾丸和中枢神经系统中也有存在。血浆中的转铁蛋白供应机体绝大部分组织的铁,而在其不能到达的部位,如卵巢、睾丸和中枢神经系统等,则由这些组织自己合成的转铁蛋白在局部产生转铁作用。
转铁蛋白于1945年首先在人血清中发现,后在猪等哺乳动物以及鱼类、两栖类和爬行类的血清中也有发现。虽然不同种属的转铁蛋白间差别较大,但其氨基酸序列上有很强的保守性。
人类转铁蛋白由两个结构相似的分别位于N-端和C-端的球形结构域组成,为单一糖蛋白肽链,共含678个氨基酸残基,分子量约为80kD,等电点为5.9。每个转铁蛋白分子能可逆性地结合两个三价铁离子(Fe3+)。
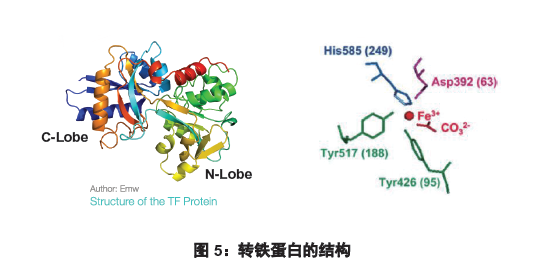
人转铁蛋白的基因位于第3号染色体q21-25上,含17个外显子和16 个内含子,mRNA长2318 bp。血浆转铁蛋白主要在肝脏合成,最初合成的转铁蛋白被蛋白水解酶分解,去掉19-22个氨基酸后方能成为成熟的转铁蛋白。
转铁蛋白对细胞发挥的作用是通过与其受体,即Transferrin Receptor(TfR)相互作用而实现的。TfR 是一种表达于细胞表面的糖蛋白,由两个同源二聚体的亚基通过二硫键连接而成。如图6,胞外负载有两个三价铁离子(Fe3+) 的转铁蛋白(Fe2 -Tf ) 与细胞(如骨髓中的网织红细胞)表面的TfR 结合,藉受体介导的内吞作用进入细胞的内体(endosome)中。内体在膜质子泵的作用下酸化,其内pH 值会下降到5.5,转铁蛋白两个小亚基上的赖氨酸(209 位和301 位)被酸化,启动双赖氨酸开关机制,迫使两个小亚基分开并释放出Fe3+,然后在还原酶的作用下,Fe3+被还原成Fe2+,再由膜二价金属转运体DMT1 转运至细胞质。释放了Fe3+的脱铁转铁蛋白与其受体组成的复合物经胞吐作用回游到细胞质膜。在细胞外,转铁蛋白与其受体解离,成为游离的脱铁转铁蛋白(Apo-Tf),然后可再与Fe3+结合后重新参与铁循环。细胞内的Fe2+被血红素、细胞色素等结合或被铁蛋白螯合作为储备铁备用[7]。
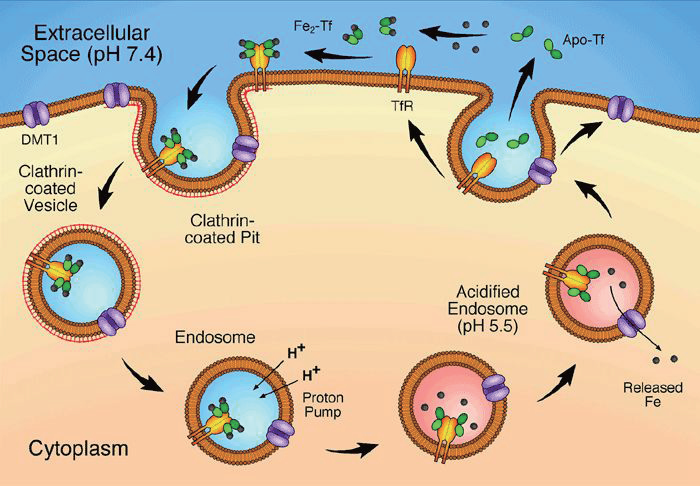 |
| 图6:转铁蛋白循环 |
2. 转铁蛋白在无血清培养基中的作用?
牛血清中含有牛种属的转铁蛋白,由于转铁蛋白的保守性,牛转铁蛋白可对人和动物细胞起到很好地保护和支持作用,因此培养基中通常要加入牛血清从而组成完全培养基。无血清培养基为达到与含血清培养基相同或相似的细胞培养性能,其中也必须添加转铁蛋白,以实现对细胞铁离子平衡的调节,以及对细胞生长和增殖的维持。
转铁蛋白在无血清培养基中具有非常重要的作用,具体包括:
1) 避免细胞外环境中自由基的产生,防止细胞受到伤害
我们知道,自由基对细胞膜、蛋白质和DNA 均有较大的损伤作用。如果细胞培养基中出现过多的自由基,被培养的细胞则容易受到伤害,而铁正是形成自由基的罪魁祸首之一。
Fe2+ + H2O2 Fe3+ + OH- + •OH
从上面的反应式可以看出,Fe2+能使过氧化氢(H2O2)还原生成羟基自由基(•OH),而羟基自由基是最为活跃和作用最强的氧自由基,对细胞的伤害很大。
转铁蛋白可以与铁离子高亲合力结合,当被添加入无血清培养基后,在细胞外的培养环境中基本不会存在游离的铁离子,也就不会发生自由基反应,故可避免自由基对细胞的损伤。
2) 维持细胞的生长和增殖
我们对转铁蛋白的转铁作用都很了解,但其实转铁蛋白更重要的意义在于维持细胞的生长和增殖,也就是说,转铁蛋白有类似于生长因子的功能。
那么转铁蛋白是如何发挥维持细胞生长和增殖的作用呢?其实这还是与其转铁功能密切相关。
我们知道,细胞内有很多重要的蛋白(见表7)需要结合铁离子后才能发挥其活性,这些蛋白基本上都与DNA 的复制和修复,以及DNA 的稳定性有关,也就是说它们影响着细胞的生长和增殖。
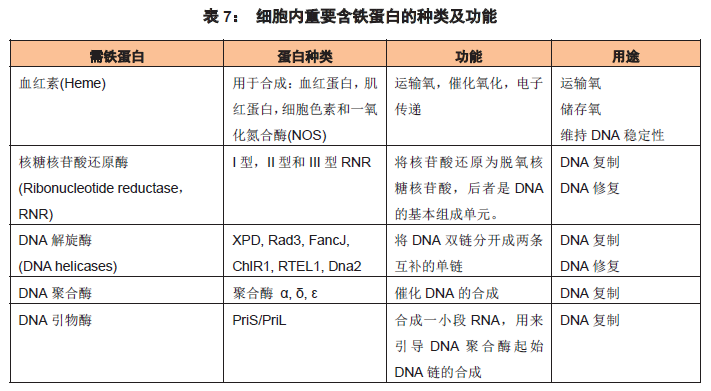
转铁蛋白通过与其在细胞表面的受体结合,将铁离子转运并释放到细胞内后,这些铁离子会与上述需铁蛋白结合,然后发挥后者维持细胞生长和增殖的功能。如果无血清培养基中不含转铁蛋白,细胞内的需铁蛋白将无法获得铁离子,因而会失去活性,导致细胞生长停滞或死亡。
3) 维持细胞内的铁平衡
转铁蛋白的这个功能也很重要。对于细胞而言,并不是铁越多越好,而应当是在适当的时间获得适量的铁。如果细胞内的铁过多,也跟细胞外环境一样,铁会诱导产生破坏力极强的羟基自由基。而如果细胞内铁过少,则不足以维持细胞的生长和增殖。
那么转铁蛋白是如何调节细胞内的铁平衡的呢?这与细胞表面的转铁蛋白受体有关。
细胞表面转铁蛋白受体的数目不是固定不变的,而是随着细胞对铁的需求程度而上调或下调,因而可自主影响细胞对铁的摄取量。
一般而言,静止未活化的细胞表面转铁蛋白受体相对较少,而活化增殖的细胞表面转铁蛋白受体数目显著增加。如淋巴细胞在有丝分裂因子的刺激下会发生转化,在DNA 合成前数小时,转铁蛋白受体的数目明显上调,铁摄入也相应增加。而到了有丝分裂期,淋巴细胞表面转铁蛋白受体数目又明显减少,这时细胞对铁的需求量也降低了。肿瘤细胞均为快速增殖的细胞,所以相对于正常细胞,肿瘤细胞表面存在着大量的转铁蛋白受体,以满足肿瘤细胞对铁的大量需求[8]。
此外,在细胞培养中,转铁蛋白受体数目与培养环境中铁的含量也密切相关。培养环境中的含铁介质比较多,则细胞表面转铁蛋白受体的数目会减少,从而避免细胞摄入过量的铁[8]。既然转铁蛋白的作用仅是向细胞内转运铁离子,然后通过铁离子来发挥维持细胞生长和增殖的作用,于是有研究者试图在无血清培养基中加入铁离子螯合剂,以将铁离子转运到细胞内,从而供细胞的生长所需,这样可以避免使用转铁蛋白,使配制出无蛋白成分的无血清培养基成为可能。铁离子螯合剂虽然也取得了部分成功,但对于绝大多数细胞并不能很好地维持细胞的生长,原因是铁离子螯合剂只有转铁作用,但无调节铁平衡的能力,常会导致细胞内的铁含量过多,进而产生自由基并使细胞受到损伤[9,10]。
3. 无血清培养基中应该添加提取的转铁蛋白,还是重组的转铁蛋白?
人血浆中转铁蛋白的含量丰富,约为25mg/ml,占血浆总蛋白的4%,而且转铁蛋白的种属间交叉活性比较强,所以转铁蛋白多从人或牛的血浆中提取而得。
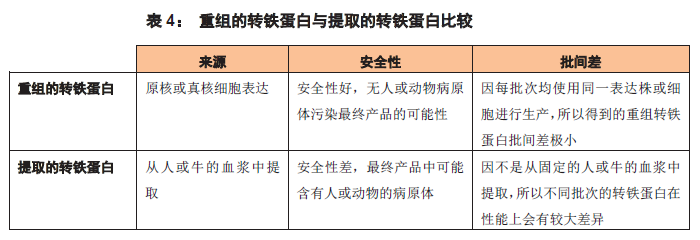
但提取的转铁蛋白具有安全性差和批间差大等缺陷(表4)。尤其是将提取的转铁蛋白添加于用于细胞治疗的无血清培养基中时,可能会将人或动物的病原体(如疯牛病病毒,克雅氏病毒和其它未知病原体)藉回输人体的细胞而带入人体,从而发生非预期的疾病。而重组的转铁蛋白,则可完全避免人或动物病原体污染的可能性,因此更适合用于配制细胞治疗用的无血清培养基。
4. 无血清培养基中应该添加铁饱和(Holo)的转铁蛋白,还是脱铁(Apo)的转铁蛋白?
我们知道,一个转铁蛋白可以高亲合力结合2 个Fe3+。结合了2 个Fe3+的转铁蛋白,因其铁离子结合位点均已被占用,所以称为铁饱和转铁蛋白,英文为Holo-transferrin,holo是全部、完全的意思。而未结合Fe3+的转铁蛋白则称为脱铁转铁蛋白,英文为Apo-transferrin,其中Apo 是分离的意思。
重组的转铁蛋白最初均为Apo-transferrin,要得到Holo-transferrin 则需在酸性环境下与一定量的六水硫酸铁铵作用,然后再将pH 值调至碱性,再作用一段时间即可。体外细胞培养时,Apo-transferrin 与细胞表面转铁蛋白受体的亲合力很弱,但当其结合细胞外环境中的Fe3+形成Holo-transferrin 后,与细胞表面转铁蛋白受体的亲合力显著提高,进而介导了对铁的转运。
那么在配制无血清培养基时,是应该添加Holo-transferrin 还是Apo-transferrin 呢?
无血清培养基中多数都添加Holo-transferrin,因为Holo-transferrin 除发挥转铁作用外,自身即可作为细胞的铁源,无需在培养基中另加外源性铁。但在某些本身含铁量高的培养基(如DMEM/F12)中,则可使用Apo-transferrin 这种不含铁的转铁蛋白。
另外需要注意,通常我们无法从理论上推断出到底是Holo-transferrin 好还是Apotransferrin好,最准确的方法是进行实验测试。
有报道在神经细胞无血清培养时,添加物B27与Holo-transferrin 合用会比与transferrin合用获得更好的神经元培养质量[11]。而另一种添加物N2,与Apo-transferrin合用时则会提高某些神经干细胞的增殖能力。
5. 转铁蛋白在无血清培养基中的使用浓度
细胞种类不同,对转铁蛋白的需求量也不同,下表谨供参考。具体的浓度还是要根据细胞的种类、状态和想要实现的功能来通过实验确定。

【参考文献】
[1] Kahn CR. The molecular mechanism of insulin action. Annu Rev Med. 1985; 36:429-51.
[2] Armitage WJ and Mazur P. Toxic and osmotic effects of glycerol on human granulocytes. Am J Physiol. 1984; 247(5 Pt 1):C382-9.
[3] Leibovich SJ and Polverini PJ. Protamine sulfate inhibition of serum-induced mitogenic responses: differential effects on normal and neoplastic cells. J Natl Cancer Inst. 1984; 73(6):1337-47.
[4] Osman IF, Baumgartner A, et al. Genotoxicity and cytotoxicity of zinc oxide and titanium dioxide in HEp-2 cells. Nanomedicine (Lond). 2010; 5(8):1193-203.
[5] 王源源等。苯酚致V79 细胞毒性及DNA 损伤效应的研究。工业卫生与职业病,2011;(2):78-81。
[6] Rowe RC, Sheskey PJ, et al. Handbook of Pharmaceutical Excipients (sixth edition). Pharmaceutical Press. 2009; p485-6.
[7] 张豪等。转铁蛋白/转铁蛋白受体介导的药物运输。中国生物工程杂志,2004;24(6):1-5。
[8] 肖芒等。转铁蛋白和转铁蛋白受体。国外医学输血及血液学分册,1987;10(4):203-6。
[9] Kovar, J and Franek F. Growth-stimulating effect of transferrin on a hybridoma cell line: relation to transferrin iron-transporting function. Exp Cell Res. 1989; 182(2):358-69.
[10] Eto, N, Yamada K, et al., Development of a protein-free medium with ferric citrate substituting transferrin for the cultivation of mouse-mouse hybridomas. Agric Biol Chem. 1991; 55(3):863-5.
[11] Chen Y, Stevens B, et al. NS21: re-defined and modified supplement B27 for neuronal cultures. J Neurosci Methods. 2008; 171(2):239-47.
附录:
| 产品名称 | 货号 | 来源 | 规格 | 价格(¥) |
| 重组人胰岛素 Recombinant Human Insulin |
10-365 |
毕赤酵母
Pichia Pastoris |
1g | 7000 |
| 5g | 28000 | |||
|
重组人转铁蛋白
Recombinant Human Transferrin |
10-366 |
水稻
Oryza Sativa |
1g | 4900 |
| 5g | 35000 | |||
|
Recombinant Human IGF-I LR3
(别名:Long R3 IGF-I) |
100-11R3-200 |
大肠杆菌
E.coli |
200ug | 1050 |
| 100-11R3-1000 | 1mg | 2830 |
