
发表日期:2021年12月13日
样本类型:人脐静脉内皮细胞(1×10^7)
研究方法:miRNA pull down、双荧光素酶报告实验、环状RNA RT-qPCR
文章链接:A circular intronic RNA ciPVT1 delays endothelial cell senescence by regulating the miR-24-3p/CDK4/pRb axis
研究思路
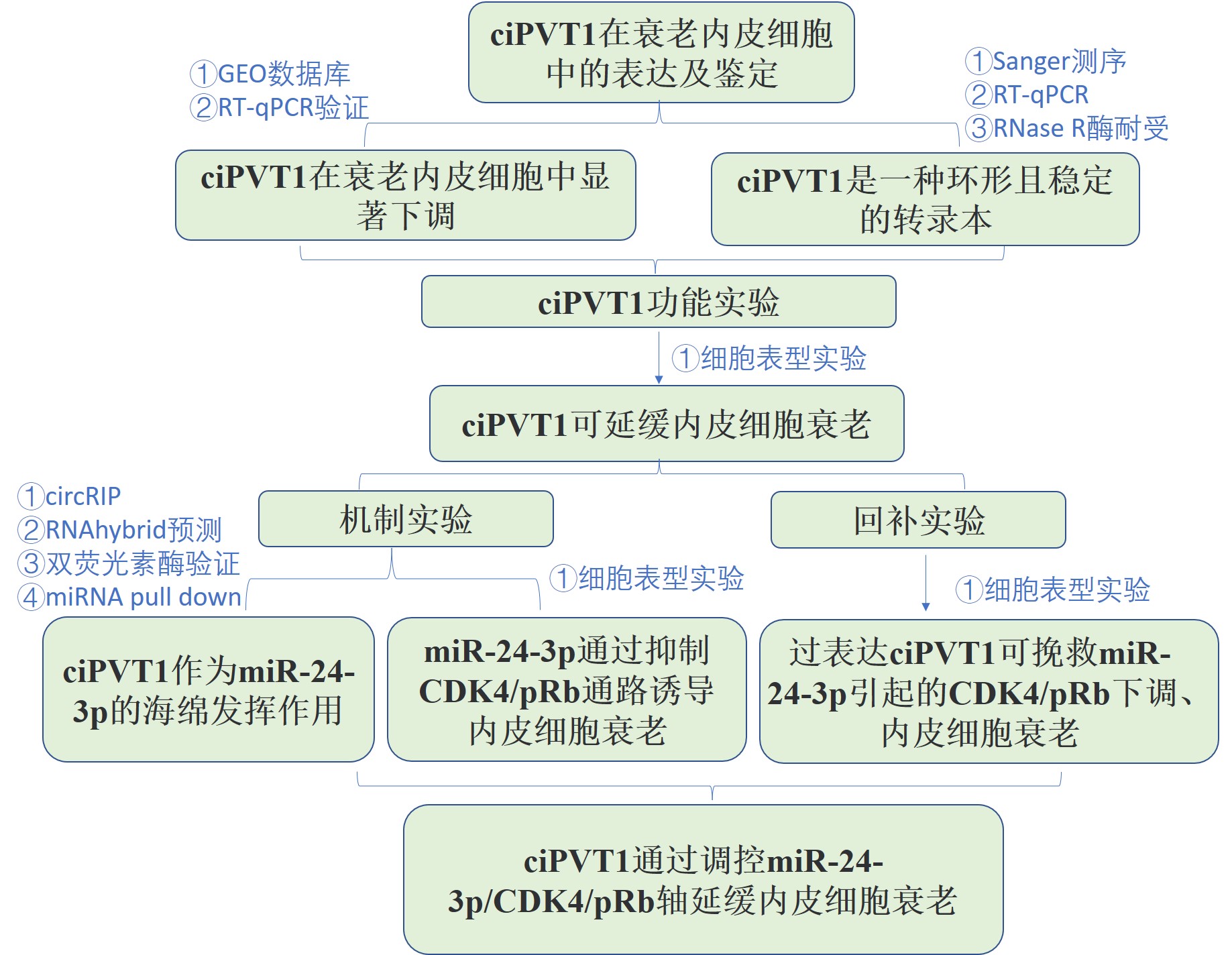
研究背景
内皮细胞排列在血管的内表面,形成一个具有多种功能的保护屏障,包括维持血管稳态、调节血压、促进血管生成和控制凝血过程。与其他正常的二倍体细胞相似,内皮细胞具有有限的细胞寿命,并最终进入复制型衰老状态。氧化应激和炎症等刺激也可诱导和促进内皮细胞衰老。内皮细胞衰老与内皮功能障碍相关,内皮功能障碍是动脉粥样硬化和高血压的独立危险因素。因此,明确内皮细胞衰老的潜在机制可能有助于发展预防和治疗年龄相关性心血管疾病的方法。此外,随着高通量RNA测序和circRNA特异性生物信息学算法的出现,大量的circRNA陆续在哺乳动物组织中被鉴定出来。其中一些在组织中丰富、稳定且特异性表达,表明它们可能在细胞中具有调节功能。已知circRNA的作用主要是miRNA海绵、结合和隔离RNA结合蛋白、调节转录和剪接以及编码多肽或蛋白质等。多项证据表明,circRNA参与各种生理和病理过程的调控。然而,circRNA在内皮细胞衰老中的作用仍不清楚。一、内皮细胞中ciPVT1的鉴定及特性
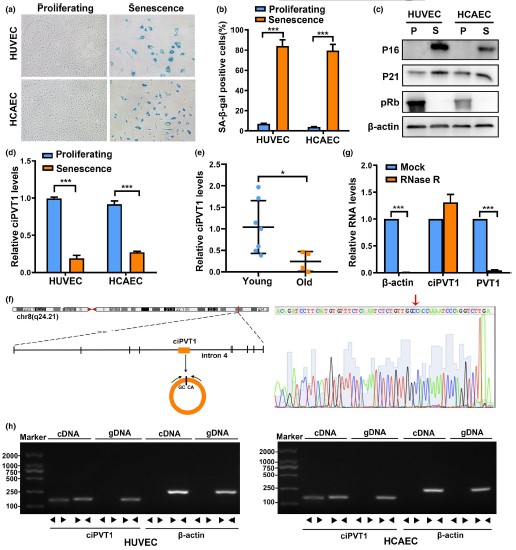
首先,作者对衰老内皮细胞的标志物进行了鉴定。衰老内皮细胞呈现扁平、增大的形态,β-半乳糖苷酶(SA-β-gal)活性增加;且pRb表达水平较低,P16和P21表达水平较高。根据之前的GEO数据库里的数据(GSE151475),ciPVT1在衰老人脐静脉内皮细胞(HUVECs)和人冠状动脉内皮细胞(HCAECs)中均显著下调,提示ciPVT1可能在内皮细胞衰老中发挥作用,那么通过RT-qPCR验证出ciPVT1的表达与RNA-seq结果一致,并且老年人的动脉ciPVT1水平明显低于年轻人。此外,作者还通过Sanger测序、RNaseR酶耐受实验以及环状RNA RT-qPCR等实验鉴定了ciPVT1的结构和序列。综上所述,这些发现表明ciPVT1是一种环形且稳定的转录本,在衰老内皮细胞中显著下调。
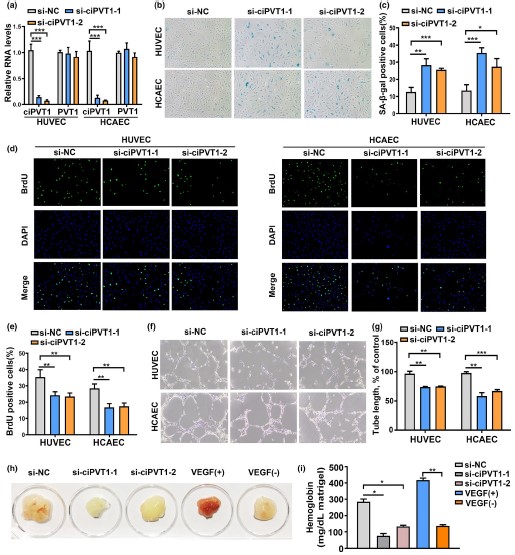
二、CiPVT1延缓细胞衰老,诱导细胞增殖,增加血管生成活性
接下来,作者研究了ciPVT1在内皮细胞衰老中的作用。敲低ciPVT1后细胞形态变大变平,同时SA-β-gal活性增加,促进了内皮细胞衰老。有证据表明,衰老的内皮细胞不能增殖,其血管生成能力受损。通过细胞增殖和体外Matrigel实验,发现ciPVT1表达的减少确实抑制了细胞增殖,并影响了内皮细胞形成毛细血管样网络的能力。此外,利用Matrigelplug(基底膜基质堵塞试验)实验进一步探究了内皮细胞的体内血管生成活性。与si-NC组相比,si-ciPVT1-转染的HUVECs显示出更少的新血管形成,且血红蛋白含量更低。综上所述,这些结果提示ciPVT1参与了内皮细胞衰老表型的调节。
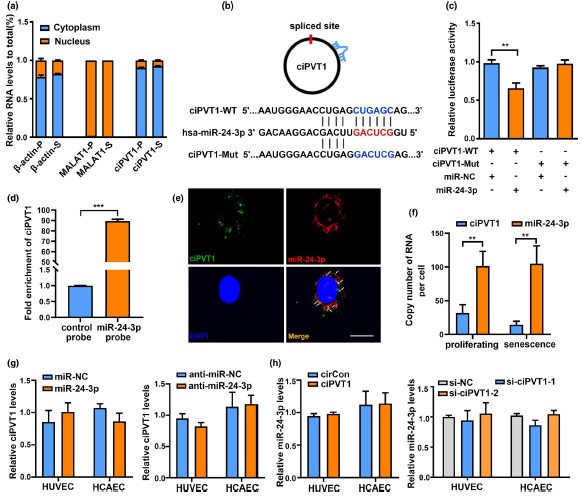
越来越多的证据表明,环状RNA可能根据其亚细胞定位发挥不同的作用。为了确定ciPVT1的细胞定位,对核和胞质ciPVT1RNA进行RT-qPCR分析。结果显示,在增殖和衰老的内皮细胞中,ciPVT1均优先定位于细胞质内,提示其转录后调控潜力。鉴于ciPVT1主要位于细胞质中,因此接下来研究了ciPVT1是否能与miRNAs结合,作为miRNA海绵。通过circRIP实验,发现miR-24-3p在circRIP实验中富集程度最高。使用RNAhybrid软件在ciPVT1序列中发现了miR-24-3p的潜在结合位点,通过双荧光素酶报告实验验证了此预测。然后,作者进一步用miRNA pull down实验证实了两者的结合;且RNA FISH检测显示,ciPVT1和miR-24-3p共定位于细胞质中。综上所述,ciPVT1作为miR-24-3p的海绵。
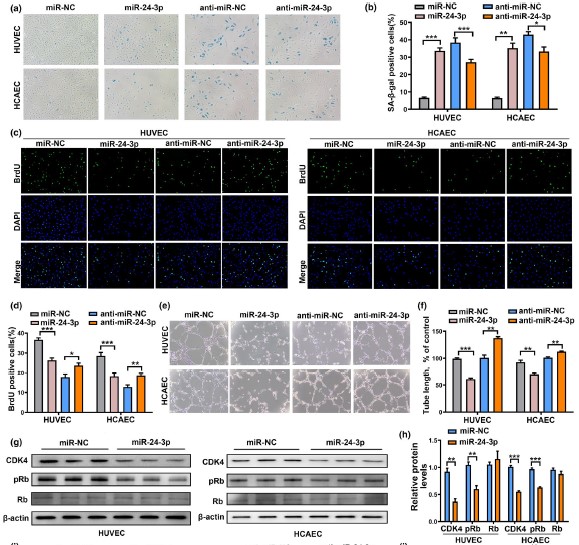
四、miR-24-3p促进细胞衰老、抑制细胞增殖和毛细血管网络形成能力
有报道称,miR-24在衰老的HDFs和HUVECs中上调,表明其在细胞衰老中的作用。作者研究了miR-24-3p在内皮细胞衰老中的作用。发现过表达miR-24-3p可增加SA-β-gal阳性细胞数量,抑制细胞增殖,损害内皮细胞血管形成能力。而敲低miR-24-3p后,衰老内皮细胞中显示相反的表型。这些结果证实了miR-24-3p在内皮细胞衰老中的关键作用。先前的研究已经证实CDK4是miR-24-3p的直接靶点。D型细胞周期蛋白/CDK4复合物能磷酸化并灭活视网膜母细胞瘤蛋白(Rb),Rb对建立衰老细胞周期阻滞至关重要。Western blot检测表明,过表达miR-24-3p可降低CDK4和磷酸化Rb (pRb)蛋白水平。这些结果表明,miR-24-3p可诱导衰老、抑制细胞增殖,并通过CDK4/pRb通路削弱内皮细胞的血管形成能力。
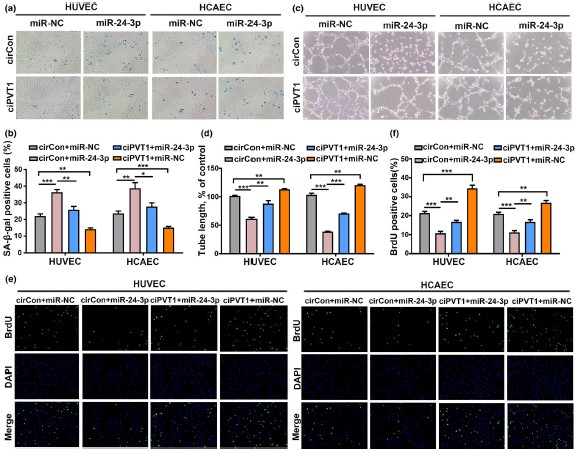
五、过表达ciPVT1可逆转miR-24-3p诱导的内皮细胞衰老
接下来,作者还探究了ciPVT1是否通过与miR-24-3p相互作用,延缓衰老、促进细胞增殖并增加血管生成活性。SA-β- gal染色显示,miR-24-3p可促进内皮细胞衰老,过表达ciPVT1可减轻这种作用。miR-24-3p可削弱内皮细胞的血管形成能力,抑制细胞增殖。同样,过表达ciPVT1可以挽救miR-24-3p过表达引起的这些表型。综上所述,这些数据表明ciPVT1通过海绵机制吸附miR-24-3p进而延缓内皮细胞衰老。
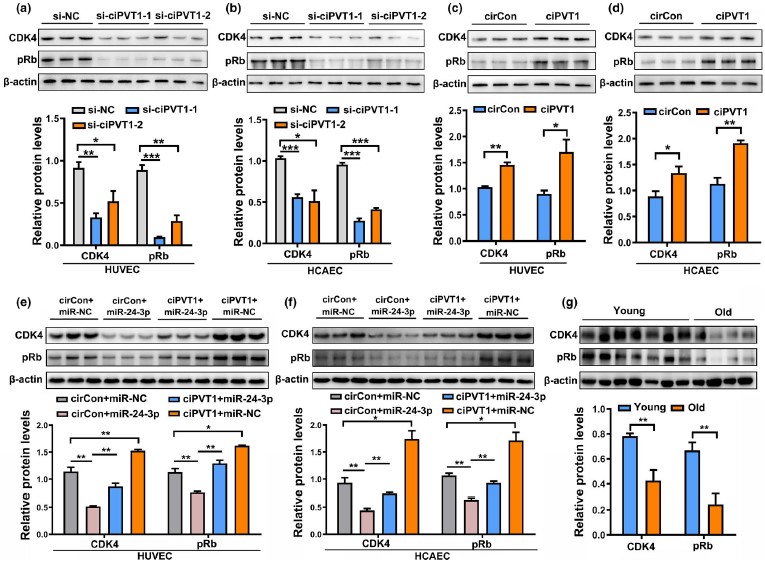
六、ciPVT1通过调控miR-24-3p/CDK4/pRb轴延缓内皮细胞衰老
由于miR-24-3p通过靶向CDK4促进内皮细胞衰老,因此假设ciPVT1通过与miR-24-3p结合,增加CDK4/pRb的水平,从而延缓内皮细胞的衰老。为了验证此猜想,检测了过表达或沉默ciPVT1后CDK4/pRb的表达。结果显示,过表达ciPVT1时CDK4/pRb上调,敲低ciPVT1时CDK4/pRb下调。接下来,作者还验证了ciPVT1是否主要通过保护CDK4不被miR-24-3p下调来延缓内皮细胞的衰老。与预期一致,miR-24-3p可以显著抑制CDK4的表达,过表达ciPVT1后抑制被延缓。表明ciPVT1通过ceRNA机制作为miR-24-3p海绵调节CDK4 。与ciPVT1的表达一致,老年人动脉中CDK4和pRb的表达水平也下调。这些结果证实了体内ciPVT1和CDK4/pRb的表达水平之间存在着相互关联。综上所述,ciPVT1至少部分通过miR-24-3p/CDK4/pRb通路延缓衰老、诱导增殖以及增加内皮细胞的血管生成活性。
环状RNA已被证实参与人类基因组的许多过程,但其在血管衰老中的功能仍在很大程度上未知。在本研究中,作者通过miRNA pull down、双荧光素酶报告实验、以及一些细胞表型实验证实了 ciPVT1在内皮细胞衰老中的功能。ciPVT1通过海绵机制调节miR-24-3p并进一步上调CDK4的表达,导致Rb磷酸化增强。此外,过表达ciPVT1逆转了miR-24-3p在内皮细胞中的衰老诱导作用。总之,本研究揭示了ciPVT1在调节内皮细胞衰老中的关键作用,并可能对寻找对抗年龄相关血管病变发展的策略具有重要意义。
云序生物作为国内早期提供环状RNA测序的测序公司,自行建立的环状RNA数据库circDB,凭借物种覆盖广、数据量大、疾病背景多的特点为客户提供优质的服务。云序积累了超过10000例环状RNA测序的经验,样本覆盖20多个物种以及50多种疾病。云序生物提供系统性环状RNA服务,从筛选(circRNA测序)到验证(qPCR)再到机制研究(RIP、RNApull-down、ChIP)以及上游表观调控(m6A甲基化等各类RNA修饰研究),全方位的覆盖环状RNA上下游分子机制验证的重要研究环节。除了提供组织和细胞的样本类型测序之外,我们还提供体液、血清血浆、外泌体石蜡样本等特殊样本的测序服务。
一、环状RNA筛选:
1.1 circRNA测序
1.2 全转录组测序(同时检测circRNA、lncRNA、mRNA)
二、环状RNA验证
2.1 qRT-PCR
对选定目标RNA分子可进行qPCR检测服务,包括引物设计与表达鉴定。
2.2 Sanger测序 与RNase R酶耐受实验
对选定的环状RNA分子进行反式剪切位点引物设计,扩增后Sanger测序验证环状;使用RNase R酶处理环状RNA分子,验证环状RNA分子稳定性。
三、 CircRNA功能机制研究
3.1 RIP测序/RIP-qPCR
针对目标蛋白抗体把蛋白-RNA复合物沉淀下来,并对复合物上的RNA进行测序或对目标RNA进行qRCR表达分析。
3.2 RNA pull-down+MS/WB/qPCR/RNA-Seq
设计目标RNA生物探针把相应的结合蛋白质与RNA复合物沉淀下来,蛋白质谱检测或WB检测与RNA结合的蛋白。设计目标RNA生物探针把相应的结合蛋白质与RNA复合物沉淀下来,qPCR检测或RNA-seq检测与RNA结合的RNA。
3.3 双荧光素酶报告实验
双荧光素酶报告实验检测两个基因之间的互作。
3.4 ChIP-seq/ChIP-PCR
检测转录因子或者组蛋白与下游基因的结合情况。
四、CircRNA修饰研究
4.1 m6A/m5C/ac4C/m7G/m1A等修饰
针对环状RNA各类修饰进行高通量筛选。
4.2 MeRIP-circRNA-PCR验证
对高通量测序的结果,通过qPCR进行进一步验证。
往期环状RNA主题回顾
经典思路|云序客户circRNA+m6A案例教您快速发表5分文章
云序用户文章|胃癌 circRNA海绵机制荣登15分杂志
2020年度circRNA研究盘点
上海云序生物科技有限公司 商家主页
地 址: 上海市松江区莘砖公路518号24号楼4楼
联系人: 戴小姐
电 话: 021-64878766
传 真: 021-64878766
Email:market@cloud-seq.com.cn;liuqingqing@cloud-seq.com.cn
